在过去的十年中,癌症免疫治疗领域取得了显著进展。免疫系统检查点抑制剂的发现和双特异性抗体、特异性阻断抗体、过继细胞疗法或细胞因子的后续使用使我们能够从不同的角度面对癌症,其中疗法使用免疫细胞识别和杀死肿瘤细胞的能力。
尽管取得了这些进展,但仍有许多类型的肿瘤对免疫疗法没有反应。肿瘤基质的复杂性、其异常脉管系统、代谢限制、免疫抑制细胞向肿瘤床的募集以及免疫抑制微环境的产生是免疫系统对其抗肿瘤作用必须面对的巨大障碍。基于自扩增RNA(saRNA)的病毒载体可以产生高和瞬时水平的转基因表达并诱导先天免疫应答,使其成为抗肿瘤治疗的有趣工具。这些载体通常以病毒颗粒的形式递送,但也可以以RNA的形式施用。
近日,纳瓦拉CIMA大学的研究人员在《分子疗法》杂志上发表了一篇题为《Intratoral
electroporation of a self-amplified RNA expressing IL-12 induces
antuminocular effects in mouse models of
cancer》的文章。研究表明,通过电穿孔局部递送saRNA可能是癌症免疫治疗的有吸引力的策略。这种方法可以很容易地转化为临床实践,特别是对于皮肤可以触及的肿瘤。
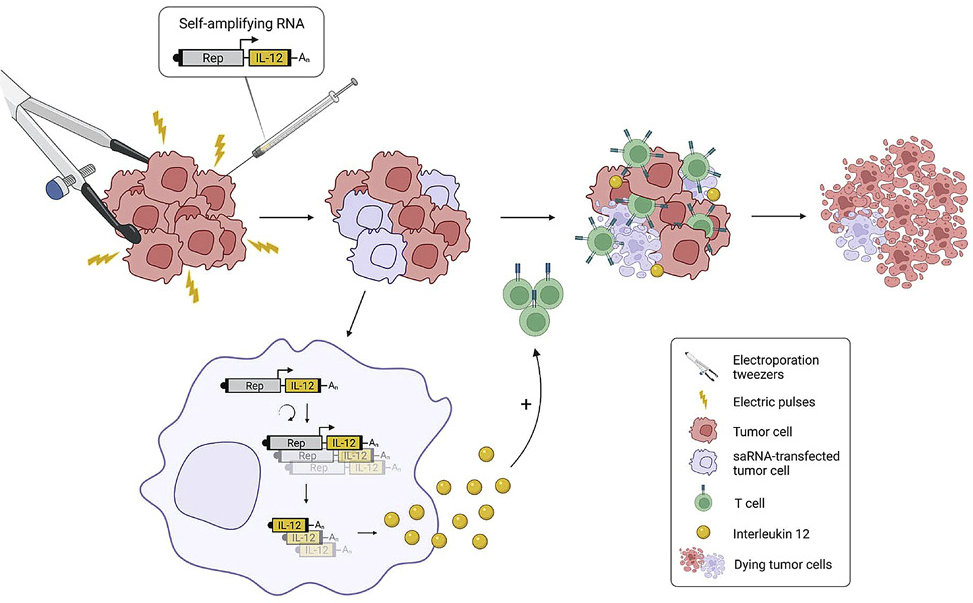
在这项研究中,研究人员通过体内电穿孔Semliki Forest病毒(SFV)saRNA以局部治疗小鼠结直肠MC38皮下肿瘤来评估这种可能性。编码荧光素酶的SFV载体用于优化肿瘤中saRNA电穿孔的条件。
然后,研究人员使用SFV
saRNA评估了这种方法的治疗潜力,SFV
saRNA编码白细胞介素-12(SFV-IL-12),这是一种具有强烈抗肿瘤作用的促炎细胞因子。通过使用我们用SFV-IL-12
RNA的最佳电穿孔条件,研究人员能够在MC 38结肠腺癌和PM299 L
HCC肿瘤中诱导显著的抗肿瘤作用。在电穿孔之前通过向肿瘤注射透明质酸酶来高度增强这种作用。这种酶可以降解肿瘤中存在的富含HA的基质,可能允许saRNA的更好分布,电穿孔后,saRNA可以接近更多数量的细胞。
事实上,研究人员之前已经观察到MC 38肿瘤可以表达PD-L1,这可能会抑制抗肿瘤反应。因此,SFV-IL-12电穿孔与抗PD-I单克隆抗体(mAb)的组合能够进一步增强该疗法的治疗效果。
先前的研究已经证明,肿瘤内递送表达抗PD-Ll的SFVVP(SFV-aPD-Ll)可诱导有效的抗肿瘤作用。因此,在未来的实验中测试电穿孔的SFV-aPD-Ll
RNA是否也可以产生治疗效果将是有趣的。总之,本研究的结果表明,通过电穿孔递送sRNA可能是局部癌症免疫治疗的一个有吸引力的策略。这种方法可以更容易地转化为临床实践,特别是对于经皮可达的肿瘤。










 实验热线:4006991663
实验热线:4006991663