近日,塔夫茨大学化学与生物工程系的NikhilU. Nair教授团队在ACS Catalysis上发表了题为“In-Depth
Sequence−Function Characterization Reveals Multiple Pathways to Enhance
Enzymatic Activity”的文章。
深度突变扫描 (Deep mutational scanning,
DMS)已成为评估序列-功能关系、识别功能热点、并加速和/或扩大工程活动的强大方法。它可以提供全面的序列-功能关系图以探索蛋白质适应度景观、发现新的功能相关位点以及确定蛋白质工程的有益突变组合。本文作者开发了一种工作流程来设计苯丙氨酸解氨酶(PAL),并进一步评估特定突变如何克服催化过程中限制活性的不同步骤,整体流程如图1所示。
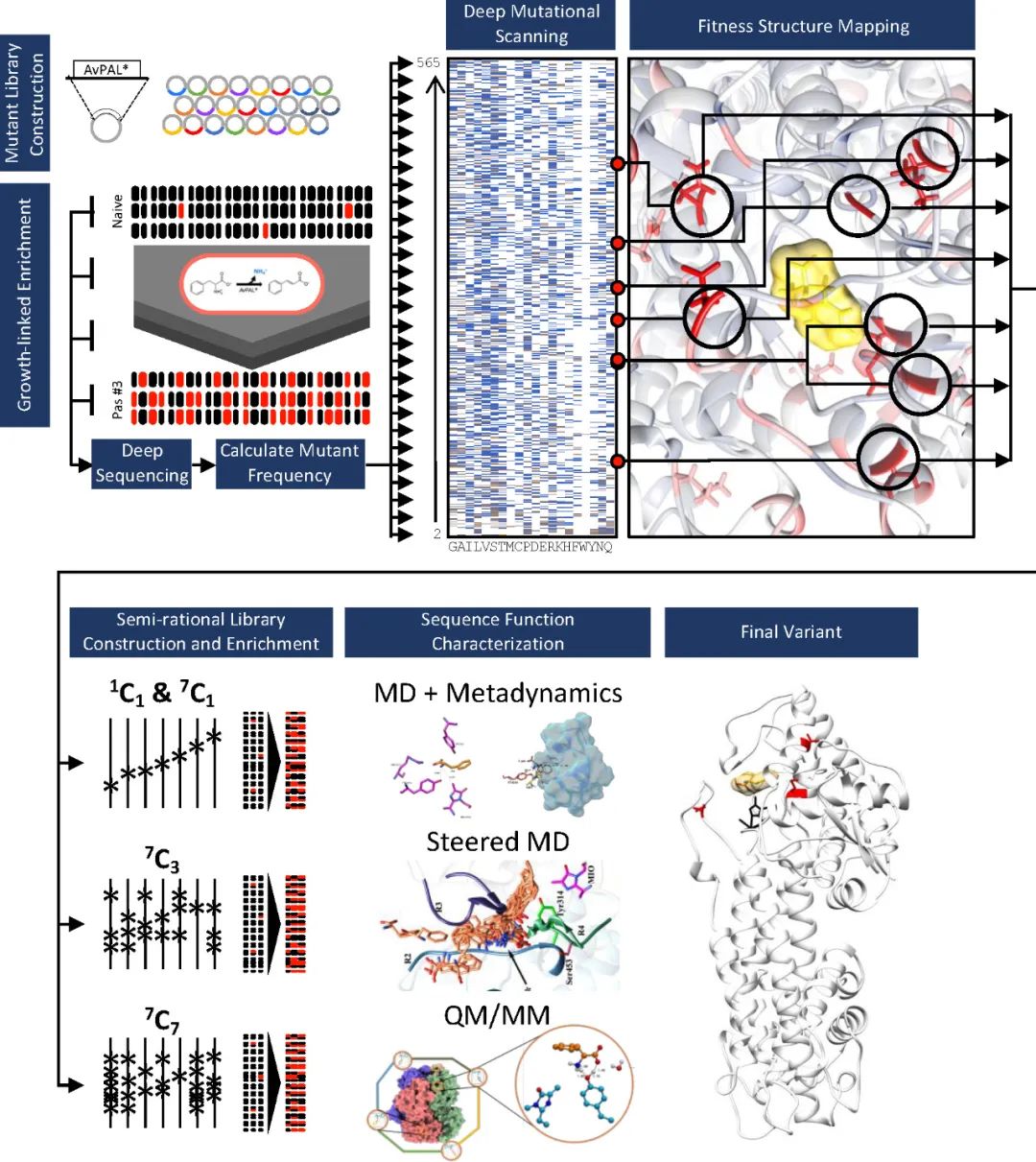
图1 工作流程
苯丙氨酸解氨酶(PAL)可将L-苯丙氨酸(Phe)脱氨基生成反式肉桂酸(tCA)和铵 (NH4+),含有4-亚甲基咪唑-5-一(MIO)加合物。PAL可用于天然产物和精细化学品的合成以及苯丙酮尿症的治疗。虽然有大量关于PAL的结构和催化机制的文献解释了底物结合口袋中的残基如何促进底物特异性和转换数,但是对如何通过突变不与底物直接接触的残基来提高酶催化性能的了解很少。
该团队此前开发了一种生长偶联富集技术,用于在大肠杆菌中快速筛选AvPAL的高活性变体。原理是高活性AvPAL变体可以更快地催化Phe脱氨生成NH4+,从而促进大肠杆菌的生长。基于此技术,作者对AvPAL进行随机突变获得了Naive文库,并传代富集了3次。然后使用高通量筛选方法对AvPAL进行DMS,获得其详细序列-功能图谱(图2)。在第3代的突变体文库中,218、222和453位点的突变高度富集(图2a)。Naive文库每个基因包含大约2-4个氨基酸突变,突变分布广泛(565个残基),每个残基平均有5.6个替换。而第3代中只有222个位置有突变,且平均只有0.6个突变(图2b)。负适应度(灰色)指的是在传代过程中出现频率下降的突变,而适应度最高的“热点”T102、G218、M222L、I268、D306、G360、N453被用于后续研究(图2c)。通过对比,作者发现适应度得分与酶的催化活性具有很高的相关性。
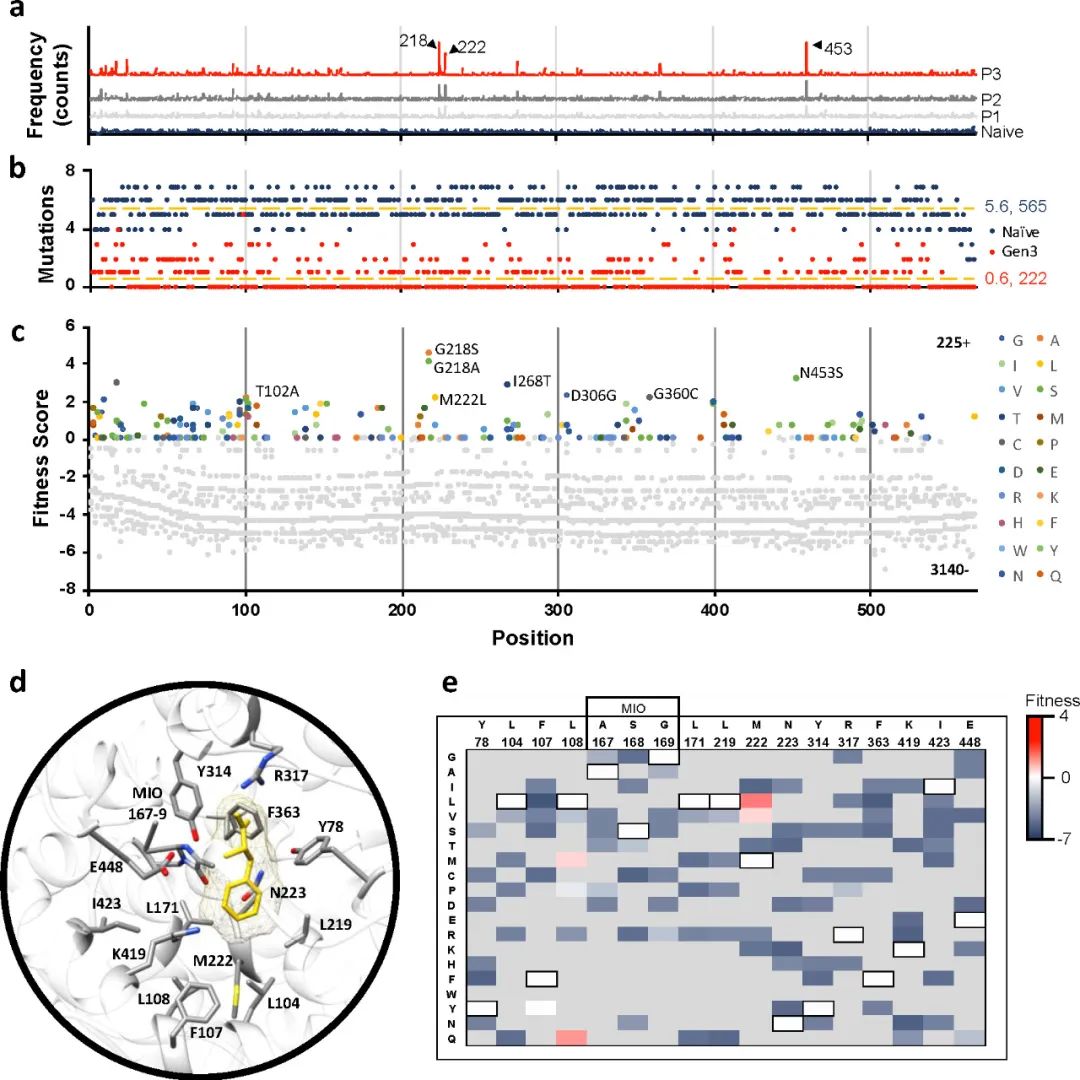
图2 AvPAL的DMS结果
作者计算了3个传代突变库相对于Naive库的适应度梯度,并将适应度映射到AvPAL蛋白结构上(图3)。AvPAL是同源四聚体,包含四个活性位点,每个活性位点由来自三个不同单体和一个MIO基团的残基组成。多数有益突变距离同一链的活性中心较远而靠近邻近链的活性中心。有趣的是,前四个突变(G218S/A、M222L和N453S)作为单位点突变的丰度最高,而三点组合突变则完全不存在,这表明有必要进一步组合研究这些热点。
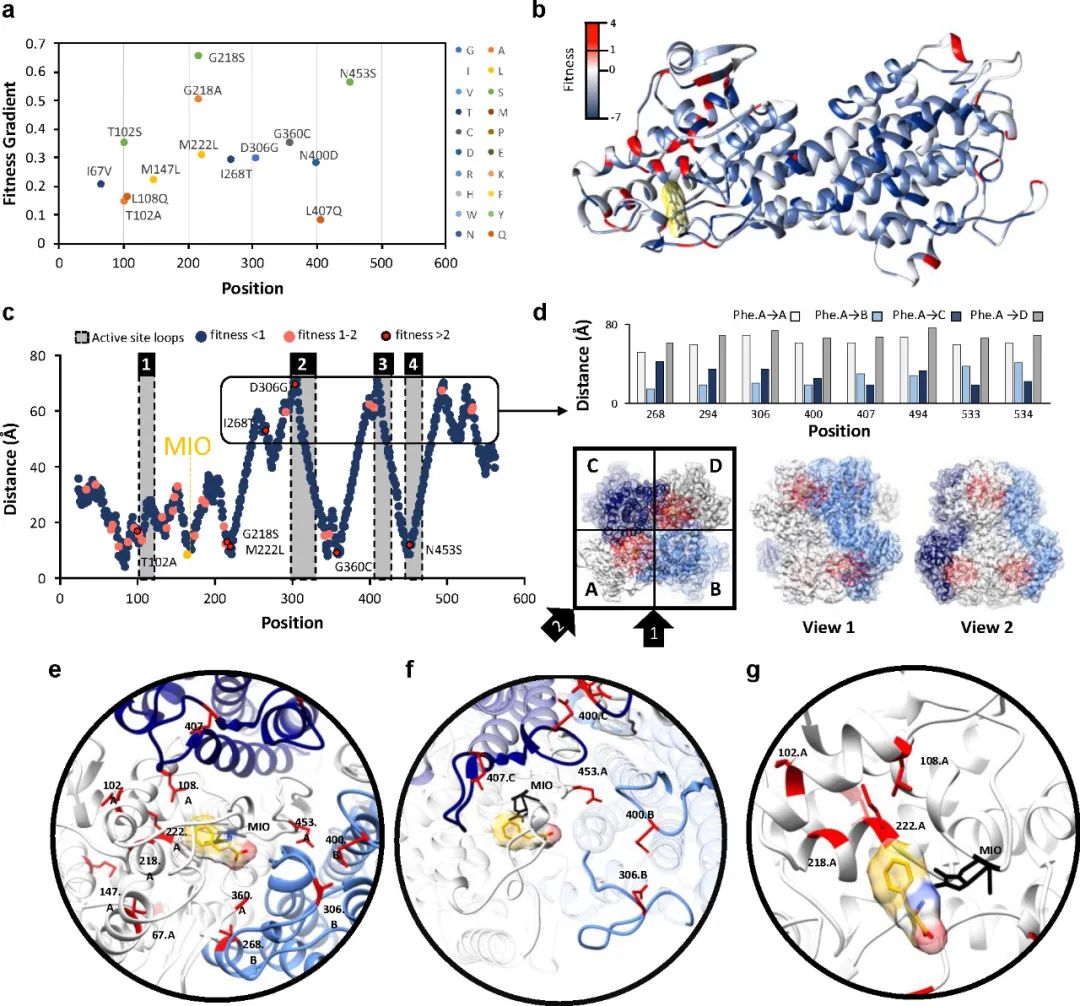
图3 识别和定位最合适的位点
作者利用7个热点分别构建了包含一个(7C1 7选1),三个(7C3 7选3),七个(7C7 7选7)位点突变的组合突变库。7C1文库中所有位点都有比野生型更适合的替换(图 4a),而7C3和7C7文库中较少的突变具有积极的适应度得分(图 4b 和 c)。这表明虽然许多突变单独有助于提高适应度,但大多数突变并不协同作用。对与AvPAL同源性最高的100个蛋白质进行序列比较,发现对于218、222、306和360位点,天然序列中完全涵盖了研究中发现的最适合的变体。而对于102、268和453位点,发现了仅通过序列比对无法预测的新突变(图4d)。其中,T102E-M222L和T102R-M222L-D306G的kcat分别显示出2.4倍和2.25倍的改进。
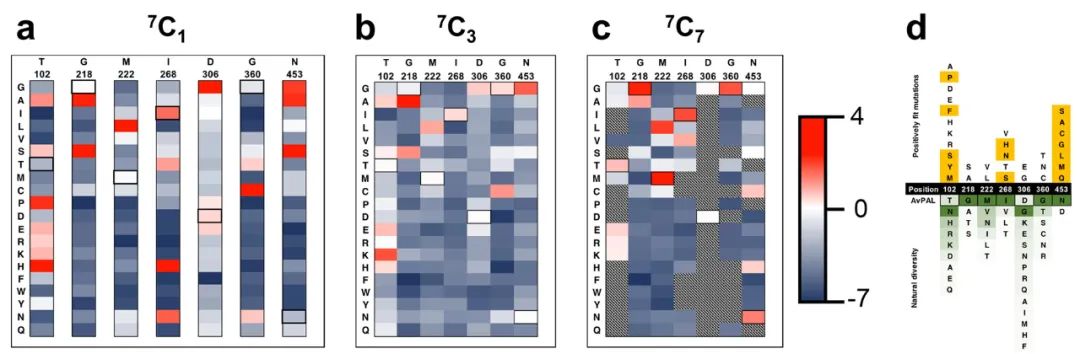
图4 饱和突变库的表征
为了揭示酶活增加的机制,作者对各突变体进行MD模拟分析。在MD模拟期间底物和催化残基之间的紧密接近表明稳定的E-S复合物和近攻击构象的形成。通过测量变体的底物氨基氮(Phe(N))与MIO亚甲基碳(MIO(Cβ2))和相邻链上314位酪氨酸羟基氧(Y314(O))之间的距离,以及对比蛋白质主链原子的均方根波动(RMSF),发现对于五种高活性变体中的四种(M222L、G218S、T012E-M222L和T102R-M222L-D306G),底物更容易接近催化位点形成稳定的近攻击构象(图5)。然而,N453S与亲本相比基本没有变化,这表明其作用方式可能不涉及直接调节底物和催化残基之间的相互作用。
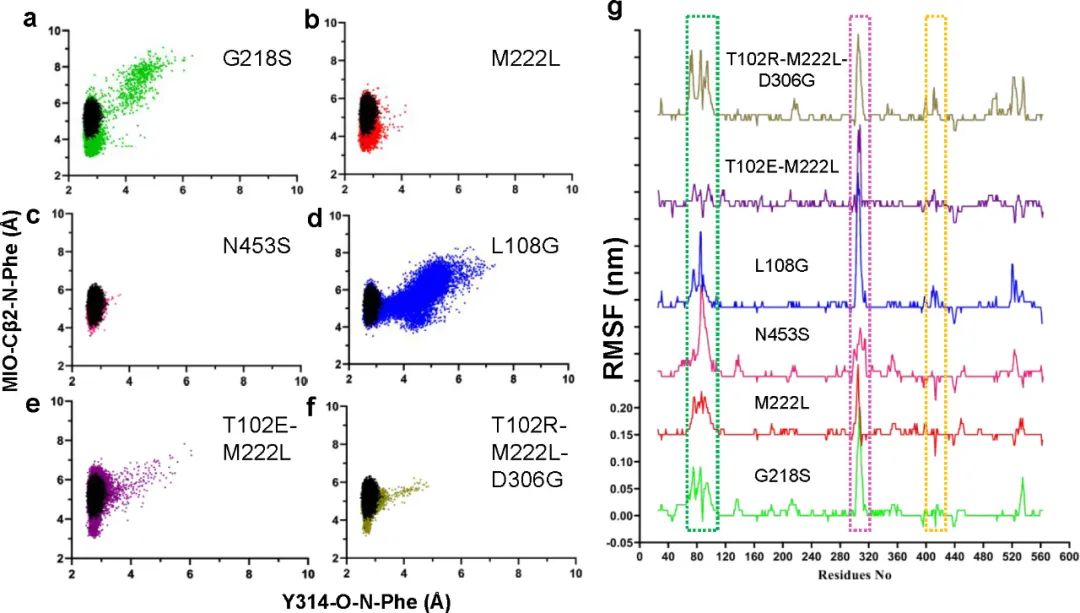
图5 MD结果分析
由于N453S位于活性位点外围,作者认为它可能会影响底物Phe的结合过程。因此,对AvPAL和突变体进行导向分子动力学(SMD)以研究Phe从活性位点离开蛋白质期间的能量变化与涉及到的相关残基。平均力势(PMF)图显示N453S有两个最小值,而在AvPAL中没有观察到(图6a)。从伞形采样中提取Phe的构象变化,并映射到AvPAL和N453S的结构上(图 6b和c)。对于AvPAL,通向活性位点的路径很窄,导致进入受限且在能量上不利。N453S的路径更宽,能量更有利,底物呈现良好的构象。
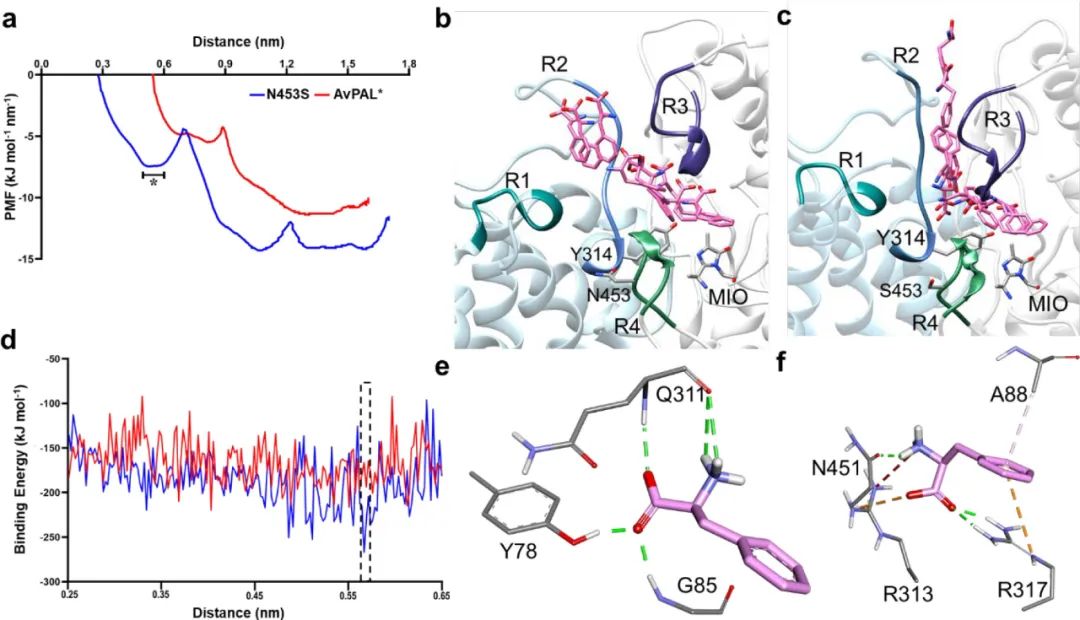
图6 AvPAL、N453S的SMD和伞形采样结果
接着作者假设N453S与其他突变体结合可能会进一步提高酶活性,并构建了M222L、L4P-G218S、T102E-M222L和T102R-M222L-D306G的N453S突变体。通过评估纯酶的动力学(图7a-e)和Phe到tCA的全细胞转化(图7f),发现添加N453S的变体都显示出与亲本相似的动力学参数,且vmax都有所降低,但T102E-M222L-N453S对Phe的转化率却提高了6倍以上。作者假设Phe可能更容易从活性位点取代 tCA从而减少了产物抑制,并随后通过添加产物的方式验证了该假设。
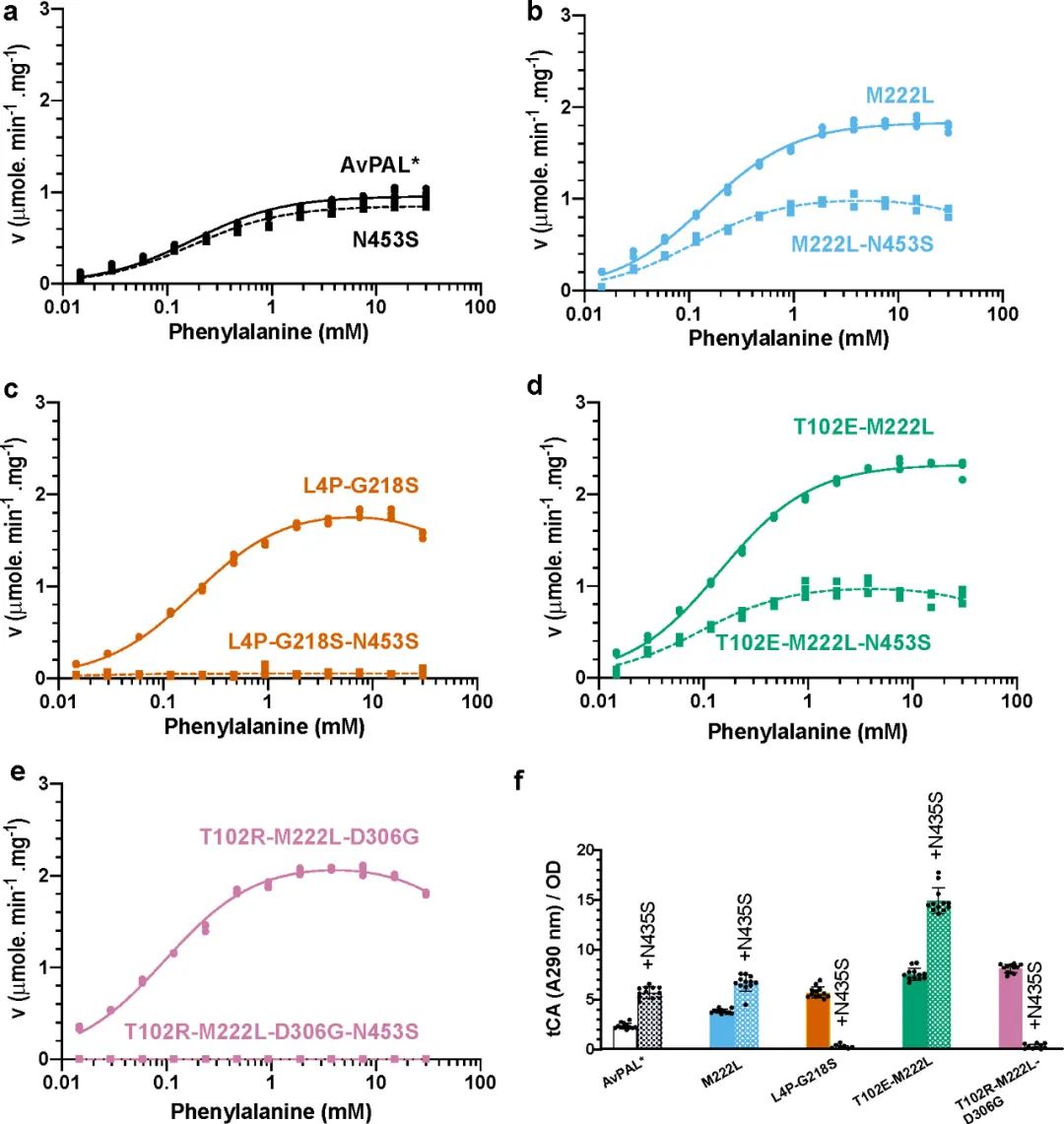
图7 N453S的动力学表征和全细胞活性
基于此前对PAL反应机制的研究,作者通过QM/MM模拟提出了AvPAL的反应机理(图8a-c),并计算出了总相对自由能图(图8d)。对比TS1和IS1的能量可以看出L108G
< AvPAL< M222L < G218S<T102EM222L <
T102R-M222L-D306G,符合实验结果。
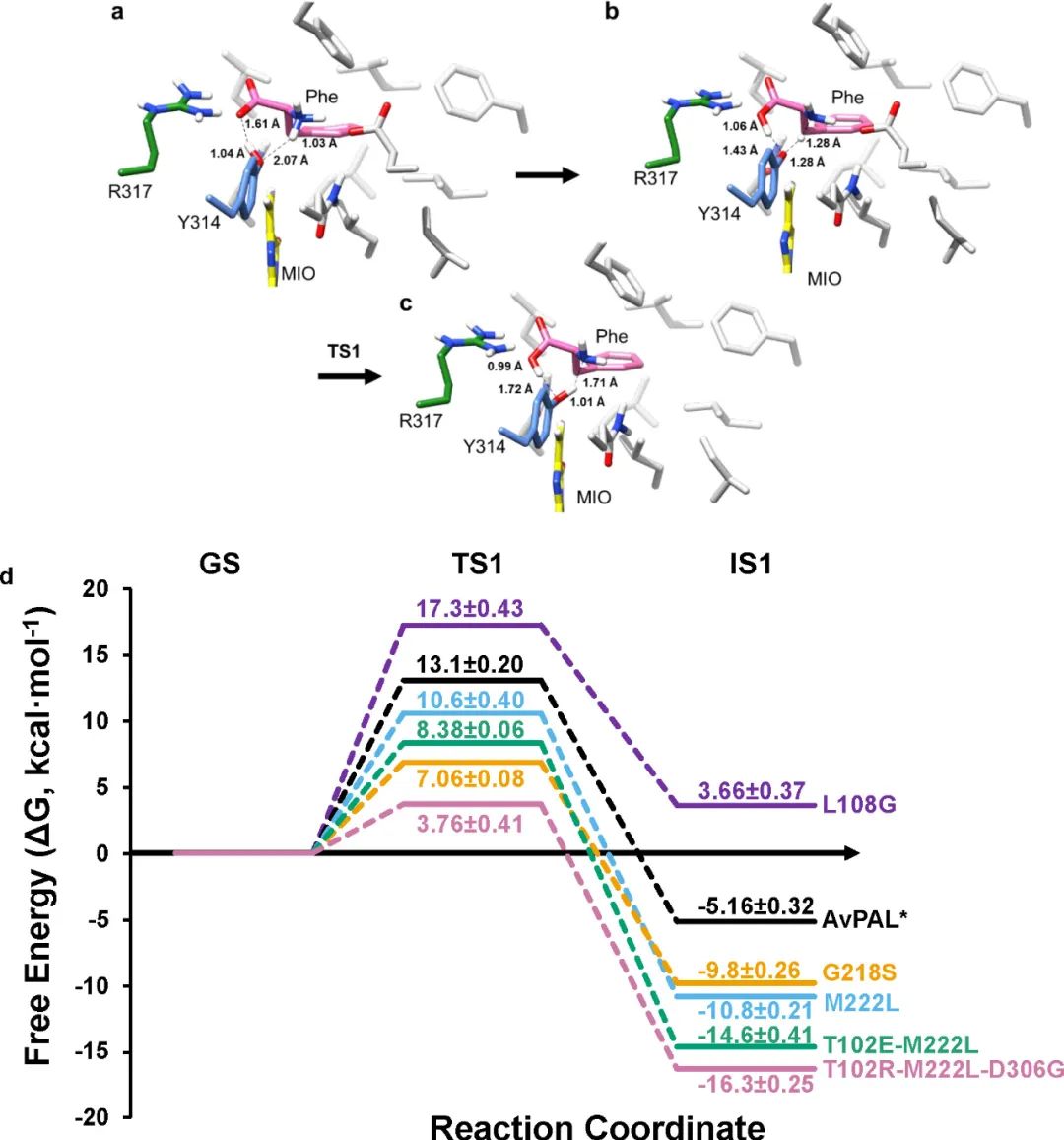
图8 对AvPAL的QM/MM研究
总之,作者报告了DMS可以指导进一步的蛋白质工程,同时也为阐明催化循环局限性的基础研究提供了起点。对含有MIO的酶AvPAL提供了最广泛的序列功能分析,并创建高活性的变体。通过计算研究(QM/MM、MD 和SMD+QM/MM),揭示了突变增强酶活性的机制,并获得更优良的突变体(T102R-M222L-N453S)。这不仅显著推进了PAL的酶学和工程学,而且还展示了使用DMS指导基础和应用酶学的能力。
辉骏实力











 实验热线:4006991663
实验热线:4006991663